生物科技研究涉及大量的细胞或者药物分子与各种电极表面之间的相互作用。由于制作方法简单且具有生物安全性,金电极被广泛应用在生物医药领域,比如:癌细胞识别以及靶向药物输送等。因此,研究金电极与各种生物界面间的相互作用有助于理解细胞识别以及药物传输机制;利用合理的方法操纵金与生物界面的相互作用也将有助于设计和制造更加有效的生物器件。
电位调控可以有效的改变金的界面性能。近年来,科研工作者已经能够利用电场快速可逆的调控金基材料的界面性能,使其在疏水和亲水状态间自由切换以及可逆控制细胞或药物分子在金表面的吸附。但金表面与细胞或者药物分子间相互作用对电场的响应机制尚缺乏理论支持。对于所有的细胞或者药物表面来说都属于亲水或者疏水状态。基于此,田煜课题组利用电化学原子力显微镜(EC-AFM)研究了亲水(SiO2)和疏水(PS)微球对金表面在不同电极电位下的粘附响应能力。研究表明,正电位下金表面的水分子定向排列会暴露出大量“悬空”的羟基,这些羟基会和亲水的SiO2 表面的羟基形成氢键进而使粘附增强;而疏水的PS表面由于没有羟基无法形成氢键,进而对电位的变化没有粘附响应能力。研究提出了一种控制粘附的新方法,有助于在癌细胞识别以及药物分子靶向输送方面得到应用。
研究成果以“Electric Potential-Controlled Interfacial Interaction between Gold and Hydrophilic/Hydrophobic Surfaces in Aqueous Solutions”发表在“The Journal of Physical Chemistry C, 2018, 122, 39, 22549-22555”上,并被选为了当期的Supplementary materials的封面文章。博士后李少伟、白鹏鹏以及博士生李远哲为文章的共同第一作者。该研究得到了国家自然科学基金(51425502),中国博士后科学基金(2018M630145),中国博士后创新人才支持计划(BX201700132)的支持。

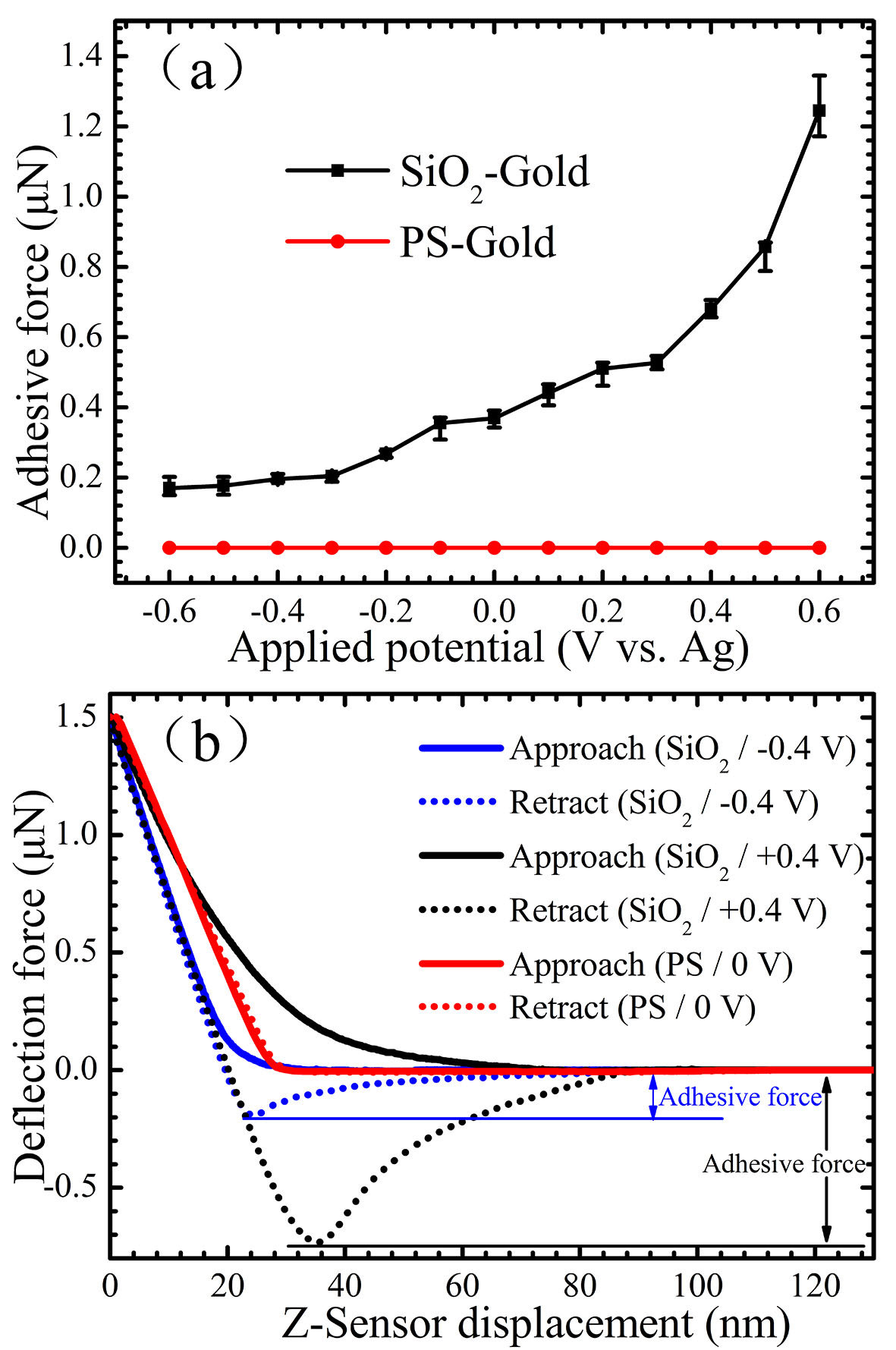
左图为以文章内容为基础的本期杂志Supplementary Materials的封面;右图(a)为粘附力随电位的变化,(b)为-0.4 V, 0 V,以及 0.4 V电位下的力曲线。


